美国首次获批:2020年5月7日
中国首次获批:未获批
获批适应症:用于治疗MET外显子14跳跃突变的晚期或转移性非小细胞肺癌(NSCLC)患者
推荐剂量:每日400mg,每日两次,口服,随餐或不随餐
【贮藏】:原包装存放于20°C至25°C(68°F至77°F),允许短期储存在15°C至30°C(59°F至86°F);注意防潮;首次打开瓶子6周后,请丢弃所有剩余的未使用的药片。
【适应症和用途】:用于治疗转移性非小细胞肺癌(NSCLC)的成年患者,其肿瘤突变导致间充质-上皮转化(MET)外显子14跳跃。
【剂量和给药方法】推荐剂量为每日两次口服400mg,饭前或饭后均可。
整片吞下,请勿打碎、压碎或咀嚼药片。
如果患者漏服或呕吐一剂,指导患者切勿补服,而是在预定时间服用下一剂。
【Tabrecta 卡马替尼(capmatinib)禁忌症】
不明确
【Tabrecta 卡马替尼(capmatinib)不良反应】
最常见的不良反应有:手或脚肿胀;恶心;疲倦;呕吐;食欲不振;某些血液检查的变化。
说明书其他节更加详细讨论以下不良反应:间质性肺疾病(ILD)/肺炎;肝毒性;
【Tabrecta 卡马替尼(capmatinib)警告和注意事项】
间质性肺疾病(ILD)/肺炎:用本药治疗的患者发生了可能致命的ILD/肺炎。监测指示ILD /肺炎的新的或恶化的肺部症状(例如呼吸困难,咳嗽,发烧)。若怀疑没有引起ILD /肺炎的其他潜在病因,请立即停止对疑似ILD /肺炎患者的本药治疗,并永久终止治疗。
肝毒性:在开始使用本药之前,应在治疗的前3个月中每2周监测一次肝功能检查(包括ALT,AST和总胆红素),然后每月一次或按临床指示进行监测,对发展中的患者进行更频繁的检查转氨酶或胆红素。 根据不良反应的严重程度,应停用,减少剂量或永久停用本药。
光敏性的风险:根据动物研究的结果,本药有光敏反应的潜在风险。在GEOMETRY mono-1中,建议患者在用本药治疗期间应采取预防紫外线照射的预防措施,例如使用防晒霜或穿防护服。建议患者在用本药治疗期间限制直接紫外线照射。
胚胎-胎儿毒性:根据动物研究的结果及其作用机理,本药对孕妇给药可引起胎儿的伤害。建议孕妇注意胎儿的潜在危险。 劝告有生殖潜力的女性及其伴侣在用本药治疗期间以及最后一次用药后1周内使用有效的避孕方法。
【Tabrecta 卡马替尼(capmatinib)在特殊人群中使用】
孕妇:根据动物研究的结果及其作用机理,当孕妇服用本药时可能引起胎儿伤害。建议具有生育潜力的女性将已知或怀疑怀孕的情况告知医护人员。建议有生育潜力的女性及其伴侣在使用本药治疗期间和最后一次服用后1周内使用有效避孕措施。
哺乳:由于母乳喂养的胎儿可能出现严重的不良反应,建议妇女在使用本药治疗期间和最后一次剂量后一周内不要进行母乳喂养。
儿科用药:本药在儿科患者中的安全性和有效性尚未得到证实。
老年人用药:临床试验中,在老年患者(65岁及以上)和年轻患者之间没有观察到安全性或有效性的总体差异。
临床数据
此次获批是基于一项多中心、非随机、开放标签、多队列研究(NCT02414139)。
该研究,共纳入了97例MET基因外显子14跳跃突变且EGFR/ALK阴性的晚期NSCLC,接受卡马替尼400mg,每天两次,口服,直到病情进展或出现不可耐受的毒性反应。
入组患者的人群特征为:中位年龄为71岁;60%的患者为女性;75%的患者为白人;ECOG评分为 0(24%)或1(75%);60%的患者无吸烟史;80%的患者为腺癌;12%的患者存在脑转移;69例经治患者中88%接受过含铂化疗。
研究数据表明:初治患者(n=28)VS 经治患者(n=69)的客观缓解率(ORR)为68% VS 41%;完全缓解(CR)为4% VS 0%;部分缓解(PR)为64% VS 41%;中位持续反应时间(DoR)为12.6个月 VS 9.7个月,持续缓解时间≥12个月的患者比例为47% VS 32%。
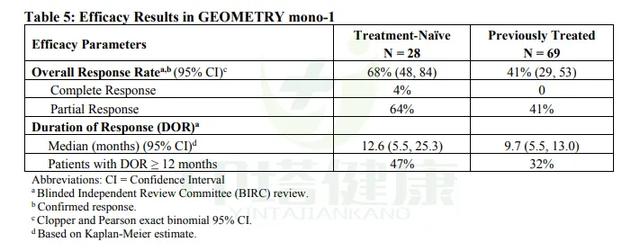 图注:卡马替尼治疗MET突变非小细胞肺癌的临床数据
图注:卡马替尼治疗MET突变非小细胞肺癌的临床数据
不良反应
常见的1~4级不良反应有:外周水肿(52%)、恶心(44%)、疲劳(32%)、呕吐(28%)、呼吸困难(24%)、食欲差(21%)、便秘(18%)、腹泻(18%)、咳嗽(16%)、非心源性胸痛(15%)、背部疼痛(14%)、发热(14%)、体重下降(10%)。
常见的3~4级不良反应有:外周水肿(9%)、疲劳(8%)、呼吸困难(7%)、恶心(2.7%)、呕吐(2.4%)、非心源性胸痛(2.1%)、背部疼痛(0.9%)、便秘(0.9%)、食欲差(0.9%)、发热(0.6%)、体重下降(0.6%)、咳嗽(0.6%)、腹泻(0.3%)。
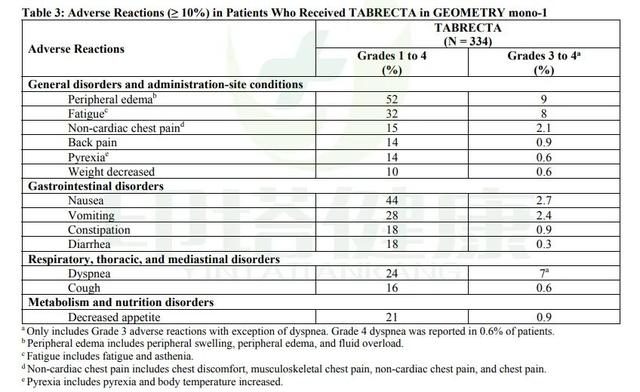 图注:卡马替尼治疗MET突变非小细胞肺癌的不良反应
图注:卡马替尼治疗MET突变非小细胞肺癌的不良反应
常见的1~4级实验室异常数据为:白蛋白减少(68%)、肌酐升高(62%)、淋巴细胞减少(44%)、丙氨酸转氨酶升高(37%)、碱性磷酸酶升高(32%)、淀粉酶升高(31%)、谷氨酰转移酶(29%)、脂肪酶升高(26%)、天冬氨酸转氨酶(25%)、低血红蛋白(24%)、低钠(23%)、磷酸盐降低(23%)、高钾(23%)、白细胞减少(23%)、低血糖(21%)。
常见的3~4级实验室异常数据为:淋巴细胞减少(14%)、丙氨酸转氨酶升高(8%)、谷氨酰转移酶升高(7%)、脂肪酶升高(7%)、低钠(6%)、天冬氨酸转氨酶(4.9%)、磷酸盐降低(4.6%)、淀粉酶升高(4.4%)、高钾(3.1%)、低血红蛋白(2.8%)、白蛋白减少(1.8%)、白细胞减少(0.9%)、肌酐升高(0.3%)、低血糖(0.3%)、碱性磷酸酶升高(0.3%)。
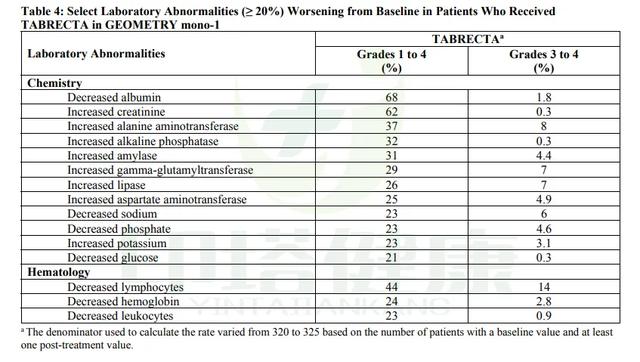 图注:卡马替尼治疗MET突变非小细胞肺癌的实验室异常数据
图注:卡马替尼治疗MET突变非小细胞肺癌的实验室异常数据
警告注意事项
间质性肺病/肺炎
在GEOMETRY mono-1临床试验中,4.5%的患者发生间质性肺病/肺炎,3级1.8%,1例患者死亡,2.4%的患者因此永久停药。3级以上间质性肺病/肺炎的中位发生时间1.4月(范围0.2月-1.2年)。
如果发现患者出现间质性肺病/肺炎的症状,如呼吸困难、咳嗽和发烧等,及时去医院检查。
肝脏毒性
在GEOMETRY mono-1临床试验中,13%的患者发生ALT或AST升高,3级以上6%,3例(0.9%)患者因此永久停药。3级以上ALT或AST升高2.7%的中位发生时间1.4月(范围0.5月-4.1月)。
服药前需检测肝功能,服药头3个月内,每二周检测一次,之后每月检测一次或据医嘱。对于ALT或AST升高患者,可增加检测次数。
存在光敏反应的风险
动物试验显示,Capmatinib有光敏性。患者服药期间应尽量减少日光照射,在室外使用使用防晒霜和防护服。
胚胎毒性
动物试验显示,卡马替尼有胚胎-胎儿毒性。患者和伴侣应在服药期间和停药一周内,使用有效的避孕措施。
注:药品如有新包装,以新包装为准。以上资讯仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。